
Seguro que habréis oido hablar de los concursos de cristalización que se realizan a lo largo y ancho de nuestra geografía. En ellos, uno de los compuestos estrella para obtener cristales espectaculares es el misterioso ADP.
No sé a vosotros, pero cuando escucho la palabra ADP siempre me viene a la cabeza, ese ATP que ha perdido un fosfato liberando la energía contenida en el enlace….
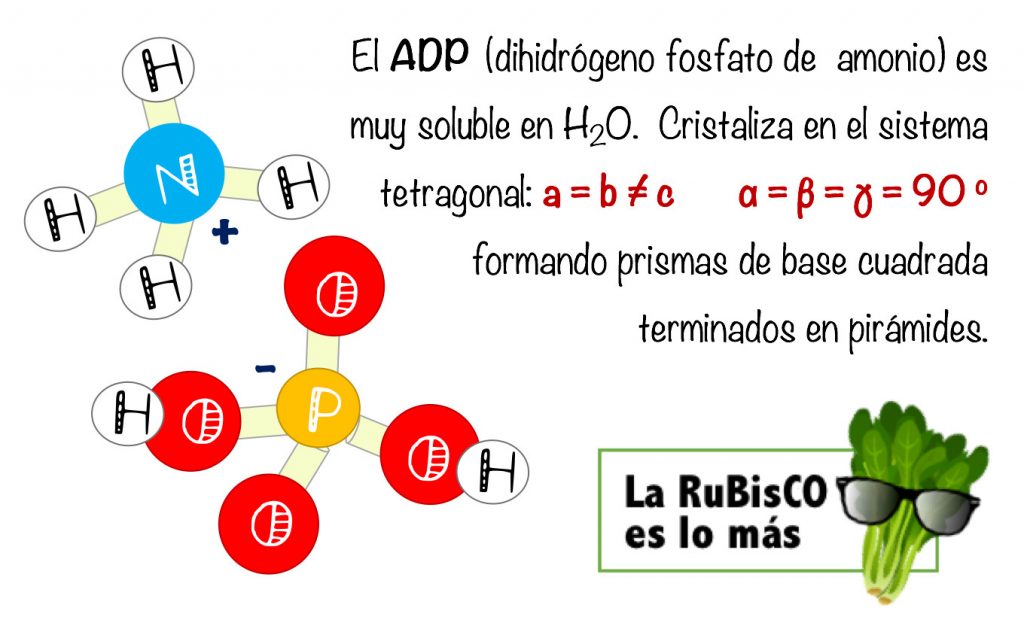
Sin embargo, además de al famoso adenosin-difosfato, las siglas ADP también pueden referirse al dihidrógeno fosfato de amonio (Ammonium Dihydrogen Phosphate, of course) también conocido como fosfato monoamónico (MAP en inglés).
En un post anterior, expliqué mis aventuras y desventuras cristalizando otras sales, ahora le toca el turno al ADP.
Materiales necesarios para obtener cristales de ADP
- ADP impuro suministrado por el concurso (también puede utilizarse el ADP puro que se usa como fertilizante, pero para que los cristales sean tan espectaculares como con el ADP impuro, se recomienda introducir un pequeño trozo de papel de aluminio en la disolución) y agua destilada.
- Diversos colorantes alimentarios y de microscopía.
-

Uno de mis alumnos ideando cómo construir un cristalizador con distintos materiales para conseguir que la Tª disminuya lo más lentamente posible Cristalizadores comerciales (de una antigua empresa llamada Triana®) y otros propios (simplemente recipientes aislantes donde la temperatura de la disolución se mantenga estable el mayor tiempo posible).
- Otros materiales: estufa, balanza de precisión, espátula, pipeta, vidrios de reloj, placas de Petri, vaso de precipitados, varilla, termómetro, trípode, rejilla y mechero Labogas®.
Protocolo sencillo para obtener la curva de solubilidad del ADP
La curva de solubilidad del ADP puro está disponible en varias páginas de Internet y publicada por la IUPAC, puedes buscar los datos aquí. Sin embargo, al estar utilizando ADP impuro (cuyo proveedor es proporcionado por los organizadores del concurso al inscribirte), resulta interesante elaborar una curva propia de solubilidad.
Para ello se realiza un montaje como el de la imagen, común a la obtención de semillas y crecimiento de cristales, en el que con ayuda de un trípode, una rejilla y un mechero Bunsen o Labogas®, se pone a calentar un volumen determinado de agua destilada en un vaso de precipitados. Si dispones de placa calefactora, la cosa se simplifica bastante.
Para realizar una aproximación a la curva de solubilidad, se puede abreviar el procedimiento tal y como explicaré a continuación.
- En una probeta, se miden 100 mL de agua destilada que se introducen en un vaso de precipitados de unos 250/500 mL. Se añade con una espátula el ADP, removiendo con una varilla hasta que la solución no admita más (a saturación), todo esto a Tª ambiente. No importa pasarse porque el exceso no va a interferir en el proceso. De todas formas, para no desperdiciar ADP ni pasarse 3 horas tirando cucharaditas y removiendo, puedes hacerte una idea mirando la curva de solubilidad del ADP puro. Por cada 100 mL se solubilizarán unos 40g de ADP a esa Tª.

- Una vez preparada la disolución, se deja reposar durante al menos 30 segundos y se coge 1 mL con ayuda de una pipeta justo del centro del vaso, intentando no remover el ADP sobrante que se ha depositado en el fondo. Ese mililitro se pondrá en un vidrio de reloj ya rotulado al efecto que habremos pesado previamente en la balanza, a poder ser de precisión (anotando su masa, of course). Para que el volumen se mantenga constante, añadiremos 1 mL de agua destilada a la disolución (*OPCIONAL).
- Posteriormente, utilizando el montaje explicado anteriormente, calentaremos ese mismo vaso con la disolución anterior hasta unos 40ºC. Una vez se acerque a esa Tª, añadiremos más ADP y seguiremos removiendo con la varilla hasta que se sature y el ADP se deposite en el fondo. Observando la curva de solubilidad, a dicha temperatura se disuelven unos 60g/100mL por lo que, habrá que añadir a los 40g anteriores (ya disueltos en el 1º paso) unos 20g por cada 100mL. Esperaremos otros 30 segundos hasta que la solución se estabilice y cogeremos otra muestra de 1 mL (restituyendo el mililitro de agua destilada para mantener el volumen en el vaso). Al añadir el ADP, desciende la Tª, por lo que, con la ayuda de un termómetro anotaremos la Tª exacta a la que extraemos la muestra de 1 mL para el 2º vidrio de reloj (también rotulado y pesado previamente).
- Volveremos a colocar el vaso en el montaje y seguiremos calentando hasta el siguiente punto de la curva, unos 55-60ºC. Repetiremos la operación, añadiendo ADP hasta saturación y removiendo con la varilla. Tras una espera de 30 segundos, cogeremos la nueva alícuota de 1 mL y la depositaremos en el vidrio de reloj nº 3 (ya pesado) introduciendo 1 mL de agua destilada en el vaso para mantener nuevamente el volumen de la solución.
- Repetiremos el proceso a los 70-75ºC, obteniendo un 4º vidrio de reloj y a 80-85ºC obteniendo el 5º y último. A partir de esa temperatura, el ADP cristaliza muy rápidamente obstruyendo pipetas a la velocidad del rayo. Es fácil recuperarlas con agua caliente pero resulta demasiado engorroso y, honestamente, mejor evitar llegar a Tª mayores que tampoco estamos haciendo un experimento crucial en el CERN.
- Llegados a este punto, tendremos 5 vidrios de reloj con 1 mL cada uno de disolución de ADP a distintas temperaturas. Los dejaremos en la estufa o en un lugar seguro hasta que el agua se evapore – y sea visible el precipitado de ADP- para, posteriormente pesarlos en la balanza. Al restar el peso del vidrio vacío (una tara a la antigua usanza) tendremos los g de ADP disueltos en 1 mL y por tanto, tras hallar la concentración en 100 mL, podremos construir una curva de solubilidad y compararla con la del ADP puro que nos proporciona la IUPAC.

Protocolo para obtener semillas de ADP
Tal y como demostraron mis alumn@s de 1ºBAC al cristalizar el azúcar en piruletas o candy rocks, la cristalización siempre se facilita si existen núcleos de cristalización. Por tanto, si obtenemos una semilla, a partir de ahí podremos obtener cristales mucho más grandes y mucho más chulos. Para conseguir semillas, una vez obtenida la curva del ADP, se pueden utilizar dichos datos o seguir las recomendaciones de la empresa que suministra el ADP impuro (cosa que hice yo finalmente para curarme en salud).
Utilizando el mismo montaje descrito, se pesan 60 g de ADP por cada 100 mL de agua destilada que vayas a usar. Nosotros solíamos utilizar unos 300-400 mL para las semillas. El ADP se debe comenzar a añadir una vez el agua esté caliente – a partir de unos 60ºC – y remover constantemente con la varilla. Siempre hay que esperar a que se alcance una Tª de 80ºC para que se disuelva todo el ADP.
Posteriormente, se mete la solución en un recipiente de plástico con tapa, ya que si es de vidrio después será imposible despegar el cristal y tendrás que disolverlo y comenzar de nuevo.
Y aquí viene el quid de la cuestión, el paso del que dependerá todo el éxito del experimento: la temperatura de la cristalización. En Secundaria, estamos acostumbrados a cristalizar por simple evaporación (como con el famoso sulfato de cobre) pero en el caso de ADP se cristaliza por enfriamiento. No soy de Física y Química, así que obviaré la explicación técnica y lo trataré de explicar con mis palabras, sorry. Para que comience la nucleación, es necesario que se llegue a la denominada zona sobresaturada (en la que el ADP ya no puede seguir disuelto y comienza a cristalizar). A esta zona se puede llegar o bien eliminando agua (la típica evaporación) o bien disminuyendo la Tª, ya que como habíamos corroborado en la curva, al aumentar la Tª aumenta la solubilidad del ADP y viceversa.
Pues bien, utilizando el mismo símil que el ponente del curso sobre cristalización del CEFIRE al que asistí:
«En un cristal, las moléculas/ átomos/ iones se organizan de forma ordenada en una estructura tridimensional. Imaginemos que nuestros alumnos entran en una clase vacía, sin pupitres, y deben colocarse en su interior de una forma ordenada. ¿Cómo conseguirán organizarse mejor, si les damos solo 10 segundos para ello o si tienen media hora para colocarse? En la cristalización ocurre lo mismo, cuanto más tiempo tarde la solución en enfriarse, la estructura formada será más perfecta y los cristales más bonitos. Es lo mismo que explicamos para diferenciar el basalto del granito».

Por consiguiente, con ayuda de tu imaginación y la de tu alumnado, hay que conseguir que la solución – en un principio a 80ºC – se enfríe lo más lentamente posible, con ayuda de estufas, cajas de porexpán o poliestireno expandido, papel de aluminio, fotocopias…
Lo que sea. Sin provocar un incendio, claro.
Los homeless o vagabundos suelen introducir papeles de periódico arrugados entre la ropa y su piel para soportar las gélidas y largas noches de invierno, just saying.
Además, con las sobras de poliestireno expandido siempre podéis divertiros disolviéndolas con un poco de acetona… Les encanta.
Por último, se deja el invento en un sitio en el que NADIE LO MUEVA (si no, se desestabiliza todo el proceso). Y al cabo de 2-3 días, al quitar el líquido sobrante (o reciclarlo) te encuentras con esta preciosidad:

Crecimiento de cristales a partir de semillas de ADP
«¿Y si a los alumnos que se tienen que organizar en la clase, les pusiéramos los pupitres bien ordenaditos? Todo seria mucho más fácil, ¿no? No hay nada como una buenas semillas para recoger una excelente cosecha».
Una vez tienes la semilla, puedes romper la pieza en varios trozos para hacer crecer los cristales a partir de dichos fragmentos. Sin meterme en explicaciones teóricas, una vez se ha dado la nucleación primaria, nos interesa que la solución se mantenga en la zona metaestable para que los cristales crezcan a partir de la semilla. Por esta razón, debes cuidar que la solución no esté en la zona subsaturada (pues entonces se disolvería la semilla en la solución) ni en la zona sobresaturada porque entonces se formarían muchísimos pequeños nuevos núcleos y cristalitos afilados sobre la semilla (y como cortan los condenados…). Por tanto la cantidad de ADP y la Tª en este paso son diferentes a la del anterior cuando obteníamos semillas.
Siguiendo las instrucciones del fabricante, esta vez se disuelven 50 g de ADP por cada 100 mL calentando a 80ºC y se deja enfriar hasta 60ºC antes de verter la solución sobre la semilla en el cristalizador. Además, es aquí donde puedes añadir diversos colorantes alimentarios, recipientes de distintas formas y… ¡dar rienda suelta a tu creatividad!


Recomiendo una prueba previa de los colorantes porque del color que se aprecia en la disolución al obtenido finalmente en el cristal va un trecho. En nuestro caso, los colorantes alimentarios típicos del Mercadona funcionaron bastante bien. Dentro de lo que cabe.
* Se puede reciclar el ADP, disolviendo cada FAIL con cristales que no han quedado todo lo bonitos que deberían. Se puede reciclar incluso el líquido sobrante en cada cristalización, tras averiguar la concentración de ADP (evaporando 1 mL en un vidrio de reloj pesado previamente como se hacía en la curva de solubilidad).
Y esto es todo. ¡Tachán!

¿Preparados para obtener, esta vez sí, cristales espectaculares?




Una duda, podríamos adicionar una sustancia fosforescente al la disolucion ? ¿ como se vería? ¿lo ha probado?
Hola
Buen dia !
Quiero ver si me podrían ayudar
Compré un fosfato monoamonico creo de baja calidad y cristaliza en forma masiva , no se hacen barras.
Ya lo he echo con otras marcas de procedencia chilena y salen bien.
Este es procedencia china !